Rudolf A. Marcus
Doctor Honoris Causa por la Universidad Politécnica de Valencia. Investido el 22 de junio de 1999
Discurso
Es un honor para mi recibir el título de Doctor honoris causa de su distinguida Universidad. Durante la mayor parte de mi vida como profesor he estado asociado con instituciones técnicas, ya que obtuve mi primer puesto académico en el Polytechnic Institute of Brooklyn y más adelante - mi puesto actual en el California Institute of Technology. De modo que me siento aquí, en la Universidad Politécnica de Valencia, como en casa y estoy orgulloso de ser honrado por ella.
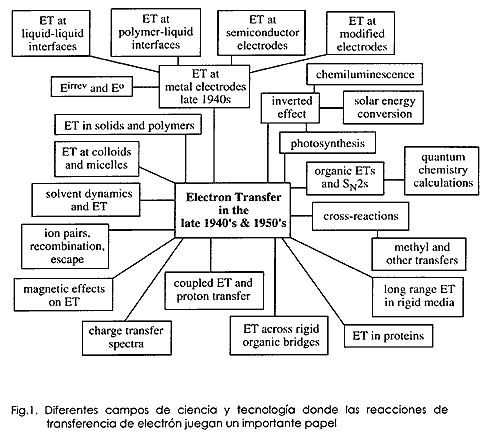
Me gustaría recordar, además, la buena interacción que he tenido con colegas españoles. Algunos vinieron a mi laboratorio para investigar y coincidí con otros en congresos o escuelas de verano. Les debo mucho por sus ideas estimulantes y por su amistad calurosa. Quisiera aprovechar esta oportunidad para describir brevemente mi investigación, así como la de otros científicos. Deseo de esa manera describir la evolución de un campo de ciencia, el de química, durante el último medio siglo. Es un ejemplo como un área diminuta de estudio escolástico que empieza como un arroyo pequeño puede evolucionar en el futuro a un diluvio de muchas ideas y áreas de investigación muy diferentes.
El campo de investigación del que hablaré hoy es el de transferencia de una partícula elemental, un electrón, de una molécula (donante) a otra (receptor). La transferencia puede ocurrir en un líquido, en una membrana biológica, o en un sólido. Esta transferencia de electrón provoca el cambio de la naturaleza química tanto del donante como del receptor, y está ampliamente presente tanto en la naturaleza como en los dispositivos artificiales. Esa transferencia participa en un paso importante en el ciclo por el que las plantas usan la energía solar produciendo oxígeno a partir de dióxido de carbono y agua. Juega un papel en la respiración de los humanos y otros seres vivos, y también en otros muchos procesos tales como la corrosión de metales, la emisión de luz por luciérnagas o a través de "lightsticks" químicos, en el funcionamiento de baterías de coches, e incluso proporciona el color a algunas piedras preciosas. Mostraré algunos ejemplos más adelante. Hoy me gustaría describirles cómo evolucionó la ciencia durante el último medio siglo en el campo de transferencia electrónica y que es lo que podemos aprender de ello.
Este campo renació poco después del fin de la segunda guerra mundial. En aquel momento los isótopos radiactivos de muchos átomos eran fácilmente accesibles. Los químicos los usaron como "marcadores" para estudiar los mecanismos de diferentes reacciones químicas, como las que permiten a las plantas utilizar dióxido de carbono para su crecimiento (Calvin, por ejemplo, recibió más tarde el Premio Nobel en Química por ese trabajo). Libby lo recibió por su trabajo sobre el trazado de carbón radiactivo que encontró innumerables aplicaciones en arqueología y antropología. Había también otros pioneros.
Un ejemplo de reacción química que incluye transferencia de electrones es el de dos moléculas cargadas ("iones") en agua:
Fe2+* + Fe3+ ® Fe3+* + Fe2+
( Ferroso* + Férrico ® Ferrico* + Ferroso )
donde el asterisco marca un átomo radiactivo que se encuentra en mínima proporción (trazas). La reacción incluye la transferencia de un electrón del ion ferroso al férrico. La velocidad de la reacción se valora separando físicamente los dos reactantes en diferentes momentos de la reacción, por ejemplo precipitando físicamente el ion férrico fuera de la solución, y analizando el nivel radiactivo de ese precipitado.
Se estudiaron muchas de esas reacciones de transferencia de electrones, abarcando muchos tipos de elementos y compuestos químicos. Esos estudios tuvieron unas consecuencias inesperadas y de mucha trascendencia, a pesar de que las reacciones de intercambio isotópico sólo eran una pequeña parte de la química:
Una razón para esas consecuencias inesperadas es que las reacciones de intercambio isotópico de transferencia de electrones representan el tipo más simple de todas las reacciones químicas. Son el tipo más simple por varias razones. Los productos finales de la reacción son los mismos que los iniciales, la única excepción es la posición del marcador radiactivo. Ese detalle significa que uno de los factores más importantes que influyen en la velocidad de una reacción química, la estabilidad de los productos frente a los reactantes, aquí está ausente. (En términos técnicos, "la energía libre estándar de la reacción", G0, es igual a cero). Además, ningún enlace químico se rompe en simples transferencias electrónicas. Por eso, los químicos que estudiaron estas reacciones pudieron dirigir su atención hacia otros factores que influyen en la velocidad de la reacción, factores que a menudo están enmascarados por el efecto de G0 y la ruptura de enlaces químicos.
De estos estudios apareció un patrón: cuando los cambios en longitudes de enlaces químicos del reactante eran grandes debido a la transferencia electrónica, o cuando los iones que reaccionaban eran pequeños, la velocidad de la reacción también era pequeña, menor en varios órdenes de magnitud, no una proporción numérica pequeña. Para interpretar ese efecto, Libby señaló que cuando el electrón "salta" del donante al aceptor, lo hace tan rápidamente que los lentos núcleos atómicos, que determinan las longitudes de enlace y la orientación de moléculas de disolvente no tienen tiempo para ajustarse a la *instantáneamente* nueva distribución de carga iónica. De esta manera pudo explicar porque la barrera energética de la reacción es más grande para los reactantes que tienen mayor diferencia de longitud de enlaces (como la diferencia entre las longitudes de enlace Fe-O en agua, entre Fe(H2O)6+2 y Fe(H2O)6+3 o una diferencia aun mayor en la "polarización dieléctrica" del disolvente que rodea cada ion. Esta diferencia de polarización dieléctrica aumenta al disminuir el tamaño de cada ion, porque un ion más pequeño crea un campo eléctrico más grande).
La dinámica idea de Libby proporcionó un salto en nuestra concepción. Sin embargo, comprendí que había un fallo. ¡Esta idea maravillosa violaba la ley de conservación de energía! Se vio claramente que la respuesta a este enigma estaba en el hecho que algunos de los cambios en la longitud de enlace y orientación de moléculas solventes tenían que ocurrir antes de la transferencia electrónica, en lugar de ocurrir todos ellos después. Basándome en esta idea, pude calcular la nueva barrera energética de la reacción y obtener ecuaciones teóricas simples para la transferencia electrónica en diferentes procesos.
Entretanto, el campo de investigación de trasferencia electrónica moderna empezó a extenderse más allá de su estrecha base, debido en parte al desarrollo de tecnología electrónica y otras tecnologías. Los sistemas de flujo rápido para el estudio de reacciones se hicieron accesibles, igual que las lámparas de flash y otras fuentes pulsátiles de luz para el estudio de trasferencias electrónicas y otras reacciones químicas. Al mismo tiempo que estos adelantos, hubo un gran desarrollo de circuitos electrónicos para el estudio de reacciones rápidas de trasferencia de electrones en electroquímica, particularmente las reacciones de trasferencia electrónica en electrodos metálicos y semiconductores y en otras interfaces.
Usando la información obtenida de las reacciones de intercambio isotópico por una parte, y la teoría que se desarrolló a partir de allí por otra, se creó una excitante colaboración entre los científicos prácticos y teóricos desde los años cincuenta en adelante. Como consecuencia, se desarrollaron estudios de trasferencia de electrones en diferentes sistemas biológicos. Se ha deducido una única ecuación para la velocidad de trasferencia electrónica, no la mostraré aquí a pesar de su simplicidad, que explicó con éxito muchos de los datos experimentales. Es aplicable a la mayoría de los fenómenos descritos en la Figura 1 de esta conferencia. En nuestra era informatizada, es fácil olvidar las grandes ventajas del uso, cuando es posible, de ecuaciones teóricas que relacionan unos fenómenos con otros. Cuando se puede desarrollar esa clase de teoría, la visión global que las ecuaciones y conceptos pueden dar al experimentador es inmensa. Pero, por supuesto, no todos los problemas tienen una solución tan sencilla.

Durante del último medio siglo los investigadores en el campo de reacciones de trasferencia electrónica incrementaron ampliamente su habilidad de medir la velocidad de las reacciones en diferentes escalas de tiempo. ¡Fueron capaces de reducir el tiempo de estudio de las reacciones por el factor de millón de millones de veces, el factor 1012! La tecnología láser jugó un importante papel en este dramático cambio en la habilidad de observar las rápidas reacciones químicas.
No creo que ninguno de los que trabajábamos en el campo de trasferencia de electrones en aquellos primeros tiempos nos imagináramos que ese tema se desarrollaría desde una diminuta semilla del estudio de reacciones de intercambio isotópico hasta el extenso área que hoy abarca; el ejemplo de este crecimiento se muestra en la Figura 1. Este increíble crecimiento se debe en parte al uso de las nuevas tecnologías, en parte al gran número de temas en los que la trasferencia electrónica juega un importante papel, y en parte a la interacción fructífera entre los científicos prácticos y teóricos. Pero el gran desarrollo mostrado en la Figura 1 no fue anticipado por nadie. (Fig 1).
Me gustaría concluir esta conferencia con algunos esquemas que describen las aplicaciones de trasferencia de electrones en diferentes aspectos de la vida humana. Están tomados de un póster preparado en Suecia durante la Semana de Premios Nobel y diseñado para explicar a un círculo amplio de oyentes la naturaleza de la investigación para la que fue otorgado el premio aquel año.
La primera transparencia es la descripción de fotosíntesis en plantas. (fig. 2).

La segunda describe la reacción química más simple, una trasferencia electrónica. (fig. 3).

La tercera describe la oxidación de metales. (fig. 4).

La cuarta el color de las piedras preciosas. (fig. 5).

La siguiente muestra la trasferencia electrónica en materia viva, (fig. 6) .
mientras que la última describe los lightsticks químicos y habla un poco sobre la teoría.
Fue una ocasión feliz que ha dejado recuerdos duraderos sobre todo lo ocurrido.
- Getting here I
- Maps I
- Contact
- Getting here I
- Maps I
- Contact
Tel. (+34) 96 387 70 00






